羟基电子式的书写
羟基(-OH)是一种常见的官能团,它由一个氧原子和一个氢原子组成,氧原子带有负电荷。在有机化学中,羟基通常与碳原子相连,形成醇类化合物。羟基的电子式表示了氧原子和氢原子之间的共价键以及氧原子上剩余的孤对电子。
羟基的电子式可以写作:
\[ \text{O}^-\text{H} \]
在这个表示中,负号表示氧原子带有负电荷。氧原子有6个价电子,它与氢原子共享2个电子形成共价键,因此氧原子上还有4个非共享的孤对电子。在更详细的路易斯结构中,孤对电子可以用点表示,如下:
\[ :O^-H \]
这里的冒号(:)代表氧原子上的孤对电子。这种表示方法更清楚地展示了氧原子上除了与氢原子形成共价键外,还有额外的孤对电子。
当羟基连接到一个碳原子上时,整个分子的电子式会根据所连接的碳原子的具体情况而有所不同。例如,如果羟基连接到一个饱和碳原子上,那么电子式会展示出碳原子与羟基之间的共价键,以及可能的其他共价键和孤对电子。
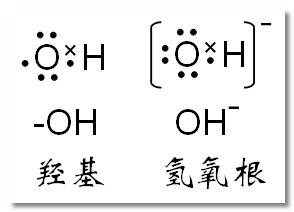
一OH电子式怎么写
OH^-(氢氧根离子)的电子式可以通过以下步骤来表示:
1. 氧原子:氧原子有6个价电子,它需要获得2个电子以达到8个电子的稳定结构。
2. 氢原子:氢原子有1个价电子,它需要获得1个电子以达到2个电子的稳定结构。
3. 形成离子:氢原子将一个电子转移给氧原子,形成OH^-离子。在这个过程中,氧原子获得了一个额外的电子,而氢原子失去了一个电子。
4. 电子式:在书写电子式时,我们通常用点(·)来表示电子。对于OH^-,氧原子周围会有8个点,表示它获得了足够的电子以达到稳定状态。氢原子则与氧原子共享一个电子对,形成共价键。
OH^-的电子式大致可以表示为:
:H
|
O⋅⋅
这里,冒号(:)表示氢原子,竖线(|)表示氢和氧之间的共价键,而氧原子周围的两个点(⋅⋅)表示它获得了额外的电子。这个表示方法是一个简化的版本,实际的电子式可能会根据具体情况有所不同。在离子中,通常会在元素符号的右上角标注电荷,以示区别。
羟基电子结构示意图
羟基(-OH)的电子结构示意图显示了氧原子和氢原子之间的化学键以及氧原子周围的孤对电子。在羟基中,氧原子有6个价电子,其中一个电子与氢原子形成共价键,剩余的5个电子中的2对(4个电子)作为孤对电子存在。以下是羟基电子结构的简化表示:
: O :
: :
H---O
在这个表示中,氧原子的两个孤对电子没有显示出来,仅用点表示了氧原子。实际的电子结构中,氧原子的两个孤对电子分别占据两个杂化轨道,而与氢原子形成的σ键占据第三个杂化轨道。在更详细的电子式中,孤对电子会被表示为未共享的电子对。
羟基由氧原子和氢原子构成,一个氧原子带8个电子,一个氢原子带1个电子,那么一个羟基带8+1=9个电子。羟基中的氢与氧之间需要共用一对电子,氧原子还差1个电子达到稳定,这也是为什么-OH不能单独存在,而是需要再连接其他基团。
如果需要更详细的电子结构示意图,通常需要专业的化学绘图软件来创建,以准确展示出氧原子的孤对电子和与氢原子形成的σ键。

 微信扫一扫打赏
微信扫一扫打赏












